Различны и многообразны причины, вызывающие боль. Разными путями поступает в центральную нервную систему болевая информация. Природа обеспечила организму максимальную надежность болевой системы. Линия передачи импульса боли необычайно сложна и проходит целую сеть промежуточных станций и подстанций, кодирующих, сортирующих и перерабатывающих поступающие сигналы. Формирование болевого ощущения начинается в рецепторах и заканчивается в нейронах коры головного мозга.
Мы уже видели, что, помимо нервных, существуют гуморальные, химические механизмы боли. Образование и накопление болетворных веществ в тканевой жидкости, окружающей рецептор, является одной из начальных стадий, предшествующих болевому ощущению. Наше сознание воспринимает его комплексно и расценивает как единое, не поддающееся расщеплению целостное чувство. Кора головного мозга интегрирует, т.е. объединяет многочисленные сигналы о физиологических и биохимических процессах, совершающихся в организме, и вызывающие в своей совокупности боль. Процессы эти можно проанализировать и разложить на составные элементы. Анализ их труден, синтез еще труднее. Но все же попробуем разобраться в цепи событий, совершающихся в организме, когда на него обрушивается сверхсильное, чрезмерное воздействие, воспринимаемое нервной системой как болевое ощущение.
В начале нашего столетия английский невропатолог Гэд предположил, что болевые нервные волокна, идущие от кожи в центральную нервную систему, несут ощущения разного характера и оттенка.
Следует указать, что задолго до Гэда, еще в 1865 г. профессор медицинской химии и физики Казанского университета А. Я. Данилевский в значительной степени предвосхитил его теорию. Изучая рефлексы на обезглавленной лягушке, Данилевский заметил, что раздражение кожи вызывает у нее два рефлекса. В первые секунды после накладывания ватки, смоченной кислотой, лягушка сгибает пальцы. Это — быстрая, почти мгновенная сигнализация. Лишь во вторую очередь, через определенный промежуток времени, наступает подтягивание лапки. Первый рефлекс Данилевский назвал «рефлексом прикосновения», второй «страстным рефлексом». Уже тогда он высказал предположение, что одно и то же раздражение передается в нервную систему разными путями.
В течение ряда лет Гэд изучал болевую чувствительность у своих многочисленных пациентов и все больше и больше убеждался в том, что существует двойная болевая сигнализация. Но больные, которых исследовал Гэд, далеко не всегда были заинтересованы в правильном диагнозе, во многих случаях такое исследование было связано с потерей заработка, переводом на другую работу, экспертизой трудоспособности и т.д. Наконец, далеко не каждый умеет рассказать о своих ощущениях, быть беспристрастным свидетелем того, что происходит в его организме.
Тогда Гэд решил поставить эксперимент на себе самом. Он предложил хирургам перерезать у него чувствительный нерв, расположенный на наружной поверхности предплечья. Эта операция была произведена 25 апреля 1903 г. Нерв был перерезан и тотчас же сшит тонкой шелковинкой.
Совершенно естественно, что область кожи, которая посылала по этому нерву свои сигналы в центральную нервную систему, лишилась связи и перестала реагировать на внешние раздражения. Наступила потеря болевой чувствительности. Строго очерченный участок кожи перестал отвечать на раздражения. Передача ощущения от кожных рецепторов в нервные клетки спинного и головного мозга была блокирована. Между концами перерезанного нерва находилась шелковинка, которая, как известно, «лишена возможности» передавать раздражения.
Постепенно, очень медленно, в течение многих недель и месяцев восстанавливалась проводимость нерва. И отдельные сигналы, поступающие из рецепторов, начали прорываться в центральную нервную систему, вызывая в ее клетках специфические болевые ощущения.
Через 8—10 недель после операции Гэд обнаружил совершенно своеобразное и довольно неожиданное явление. Легкий укол в недавно еще совсем безболезненную область стал вызывать у него чувство мучительной, почти невыносимой боли. Каждый раз, когда острие булавки касалось каких-либо особо чувствительных точек, Гэд не мог удержаться от крика. Он вскакивал, хватал за руку своего ассистента, дрожал всем телом и долго не мог прийти в себя от нестерпимой боли. В этом ощущении была одна совершенно непонятная особенность — его нельзя было локализовать, т.е. нельзя было точно установить, откуда оно идет, где расположена исходная точка, откуда начинается и куда распространяется боль.
Жестокие боли возникали при легком уколе, при незначительном охлаждении и согревании определенных участков кожи. Это болевое ощущение, появляющееся при восстановлении проводимости в нерве, Гэд назвал «протопатической чувствительностью». Под этим названием мы понимаем в настоящее время первичную основную (и в достаточной степени грубую) чувствительность. В ней нет тонкости и специфичности, она не различает отдельных раздражений, не дает точного, связанного с определенным участком восприятия. Она не локализована. Нервные волокна, по которым протопатическая чувствительность достигает центральной нервной системы, передают только грубые болевые раздражения, как, например, уколы, щипки, резкие температурные колебания и т. д.
В процессе эволюции протопатическая чувствительность появилась на самых ранних стадиях развития животного организма. Это была примитивная, далеко не совершенная сигнализация, которой располагала природа уже много миллионов лет назад. При каждом механическом раздражении кожного покрова — при ударе, ушибе, падении — из периферических рецепторов поступал в центральную нервную систему грозный болевой импульс. Он был сигналом опасности, признаком нарушенной целостности оболочки, в которую было заключено тело примитивного существа, впервые ощутившего боль.
Проходили века и тысячелетия. Совершенствовался животный организм. Возникали новые виды живых существ. И, наряду с протопатической чувствительностью начал развиваться другой вид более тонкой чувствительности, так называемой чувствительности эпикритической.
В опыте Гэда эпикритическая чувствительность начала появляться только через полтора-два года после перерезки нерва. К этому времени Гэд начал различать слабые прикосновения, небольшие колебания температуры в пределах 3—4°, незначительные раздражения кисточкой, волокном, ватным тампончиком. Он уже мог точно определить, откуда идет ощущение, умел его локализовать. Закрыв глаза, Гэд точно указывал, в какой точке нанесен укол, где он ощущает боль, а где — легкое прикосновение. Впрочем, полное восстановление наступило только через пять лет.
Если вдуматься в теорию Гэда, сразу обнаружится, что она близко соприкасается с современными представлениями о «двойной боли». И все сомнения, и возражения, возникшие в дискуссии по поводу «двойной боли», могут быть отнесены к теории Гэда.
Советские физиологи считают, что у здорового человека оба вида чувствительности дополняют друг друга, В то время как протопатическая чувствительность сигнализирует о разрушительном воздействии, эпикритическая несколько смягчает, тормозит грубое, мучительное болевое ощущение, дает возможность точно определить его локализацию. В тот момент, когда одновременно возбуждаются волокна, обладающие протопатической и эпикритической чувствительностью, возникает болевое ощущение, резко отличающееся от чисто протопатического. Оно локализовано, т.е. прочно связано с точкой, в которой возникло. Оно не носит расплывчатого, диффузного характера и ощущается до тех пор, пока длится раздражение. Как только кончилось раздражение, исчезает боль.
В настоящее время можно считать доказанным, что импульсы, поступающие от тактильных рецепторов, воспринимающих прикосновение, смягчают и ослабляют чувство боли.
Если у кошки перерезать нервные пути, передающие в центральную нервную систему чувство прикосновения и давления, животное сразу перестает ориентироваться в своих болевых ощущениях.
Попробуем сжать хвост кошки. Раздражение копчиковых нервов вызовет резкое болевое ощущение. Кошка повернет голову к хвосту и попытается освободить его от сжимающего предмета. Иначе ведет себя животное, у которого благодаря перерезке нервных путей отсутствует чувство прикосновения. Эта кошка отчаянно кричит, рвется из рук, царапается, но не поворачивает головы к месту раздражения. Она не знает, откуда идет боль и не в состоянии ее локализовать.
Опыты Гэда показали, что только гармоническое сочетание протопатической и эпикритической чувствительности дает возможность правильно реагировать на раздражение, идущее от внешних покровов; оно позволяет осмыслить то, что происходит во внешней среде и что в данную минуту вызывает у него неприятное или болезненное ощущение.
Аналогичные опыты с перерезкой кожных нервов были поставлены на собаках. Оказалось, что в начальной стадии восстановления нервной проводимости собака отвечает на малейшее раздражение отдергиванием лапы, криком и визгом.
Таким образом, протопатическая группа чувствительных нервных волокон передает в центральную нервную систему ощущение боли и грубое температурное чувство (ниже 26° и выше 37°). В то же время по эпикритическим нервным волокнам поступают сигналы, вызванные прикосновением или изменениями температуры в пределах 26-37° С.
Большинство внутренних органов обладает одной лишь протопатической чувствительностью. Если надавить на язву желудка или на больную точку, мгновенно возникает резкое болевое ощущение. Его местоположение легко определить, и врачи охотно пользуются методом прощупывания болевых точек. Это объясняется тем, что к протопатической чувствительности внутренних органов присоединяется эпикритическая чувствительность кожных покровов, через которые производится надавливание или прощупывание больного желудка, почки, печени и т.д. Однако по своему характеру эти болевые ощущения резко отличаются от мучительных, трудно локализуемых болей при почечной колике, язве желудка и двенадцатиперстной кишки, приступе желчно-каменной болезни.
Импульсы, возникающие при давлении пальцами или инструментами на кожу или больной орган, поступают в нервную систему по чувствительным волокнам через задние спинномозговые корешки, в то время как более тонкие раздражения, вызванные болезнью, разрушением ткани или воспалением, передаются в спинной и головной мозг по волокнам симпатической и отчасти парасимпатической системы. Они и рождают самостоятельные, иногда совершенно невыносимые, боли во внутренних органах.
В последние годы удалось показать, что эпикритическая и протопатическая чувствительность имеют свои собственные «пути следования» в центральную нервную систему. По толстым нервным волокнам типа А и В передаются быстрые эпикритические импульсы, а по тонким волокнам типа С — медленные протопатические. Таким образом, нервная система получает в первую очередь информацию о прикосновении и давлении, к которой лишь во вторую очередь присоединяются болевые сигналы.
Различны и конечные станции эпикритического и протопатического болевого ощущения. Центром эпикритической чувствительности является кора головного мозга, протопатической — зрительные бугры. Именно в коре головного мозга рождаются смягчающие, успокаивающие боль импульсы, при отсутствии которых самое легкое болевое раздражение превращается в стойкую, нестерпимую боль.
В клинике нервных болезней нередко приходится наблюдать появление так называемых гиперпатических болевых участков на поверхности кожи. Малейшее прикосновение к этим участкам вызывает жестокую длительную боль. Гиперпатия отличается от обычной повышенной болевой чувствительности. Мы называем гиперпатиями чрезвычайно сложные, мучительные болевые состояния, имеющие выраженный протопатический характер. Они сопровождаются тяжелыми эмоциональными переживаниями, нарушениями деятельности вегетативной нервной системы и расстройством питания тканей.
Более подробное изучение гиперпатий показало, что они возникают в результате высвобождения низших, более древних и более примитивных нервных центров из-под тормозящего и регулирующего влияния высших отделов нервной системы. Именно при гиперпатиях протопатическая чувствительность выходит из-под влияния чувствительности эпикритической.
Хотя гипотеза Гэда получила широкое распространение и до сих пор многие исследователи считают ее непогрешимой, все же неоднократно и у нас, и за границей появлялись работы, опровергающие существование как «двойной боли», так и раздельной протопатической и эпикритической чувствительности. Некоторые исследователи считают, что протопатическая чувствительность всецело находится в ведении зрительных бугров, а эпикритическая — в ведении коры головного мозга. Немецкий невропатолог Ферстер различает «чувство боли», которое он относит к протопатической чувствительности, и «ощущение боли», соответствующее эпикритической чувствительности Гэда. П. К. Анохин считает, что мучительные болевые ощущения, возникающие в процессе восстановления проводимости в нерве, зависят от того, что сигналы идут сразу по всем прорастающим нервным волокнам. Центральная нервная система как бы получает залп из многоствольного ружья. А в дальнейшем, когда проводимость перерезанного нерва полностью восстанавливается, сигналы следуют по отдельным изолированным волокнам. Поэтому на первых порах при восстановлении нерва преобладает компактное, грубое, всеобъемлющее ощущение, которое в дальнейшем становится более тонким, более точным и локализованным.
К. М. Быков также отрицает существование антагонизма между двумя формами чувствительности. Он полагает, что нельзя считать правильным утверждение Гэда о том, что в нормальных условиях корковая эпикритическая чувствительность оказывает влияние на протопатическую. Необычайная пестрота изменений чувствительности связана со сложным взаимодействием нервных центров в коре головного мозга и в зрительных буграх.
Ряд возражений против теории Гэда выдвинули английские исследователи (Люис, Троттер и Дэвис), которые пришли к выводу, что эта теория не отвечает новым экспериментальным данным, полученным за последние годы. Они установили, что после перерезки нерва восстановление чувствительности к прикосновению, давлению, теплу, холоду и боли происходит одновременно. Но в период восстановления вновь образующиеся нервные волокна обладают повышенной проводимостью и легко раздражаются при изменении химического состава и биологических свойств окружающей их тканевой жидкости,
На симпозиуме 1959 г., посвященном нервным механизмам боли и зуда, английский ученый Уиттеридж сказал, что он хотел бы, чтобы термины «протопатическая» и «эпикритическая» чувствительность были бы на несколько лет забыты.
И все же, учитывая огромное физиологическое значение боли для всей жизнедеятельности человека и животных, трудно допустить, что в организме отсутствуют факторы, способные регулировать болевое ощущение. Природа делает все возможное, говорили в древности, чтобы деревья не упирались верхушками в небо. То же происходит в животном организме. В своей книге «Кора головного мозга и внутренние органы» К. М. Быков приводит замечательную мысль Лавуазье: «Можно без устали восхищаться системой общей свободы, которую природа, казалось, хотела установить во всем, что имеет отношение к живым существам. Давая им жизнь, произвольные движения, активную силу, потребности, страсти, она не запретила пользоваться ими. Она хотела, чтобы они были свободны даже до злоупотребления; но, осторожная и мудрая, она повсюду поставила регуляторы, она заставила пресыщение следовать за наслаждением. Как только животное, возбужденное качеством или разнообразием яств, перешло положенную границу, появляется несварение, которое одновременно является предохранением и лекарством: очищение, которое оно производит, отвращение, которое оно сменяет, восстанавливает вскоре нормальное состояние животного» [14].
На каждом шагу мы встречаем подтверждение этой мысли. Наряду с симпатической нервной системой существует парасимпатическая, наряду с надпочечниками и щитовидной железой — сложный гипоталамо-гипофизарный комплекс, регулирующий их деятельность.
Когда при некоторых сильных воздействиях на организм (ранениях, ожогах, охлаждениях, инфекциях) передняя доля гипофиза усиленно выделяет стимулирующий деятельность коры надпочечников адренокортикотропный гормон и в кровь начинают поступать кортикостероиды (гормоны различных слоев коркового слоя надпочечников), тотчас же в систему физиологических регуляций вовлекаются силы, подавляющие деятельность гипофиза и тормозящие образование выделяемых им гормонов. Возбуждаются определенные отделы головного и спинного мозга, перестраивается деятельность вегетативной нервной системы и эндокринного аппарата. Все это приводит к уменьшению секреции адренокортикотропного гормона и, тем самым, к ослаблению выделения кортикостероидов. В свою очередь снижение уровня кортикостероидов в крови приводит к усилению активности гипофиза и возникновению новой цепной реакции, заново повторяющей круг описанных выше физиологических взаимодействий.
Когда болевое раздражение стимулирует деятельность симпатического отдела вегетативной нервной системы и в крови резко повышается содержание адреналина, норадреналина и других химических веществ, вызывающих выраженные симпатические реакции, в действие вступает парасимпатический отдел, ослабляющий и иногда вовсе уничтожающий проявления высокого симпатического тонуса. На какой-то стадии в крови обнаруживаются, наряду с адреналином, большие количества парасимпатического медиатора — ацетилхолина, наряду с норадреналином — гистамин и серотонин.
Во всех тканях организма можно обнаружить не только ацетилхолин, но и расщепляющий его фермент холинэстеразу, гистамин связан в единый комплекс с ферментом; диаминоксидазой, адреналин — с фенол-оксидазой, в присутствии которых эти вещества разрушаются и теряют свою активность. Фермент каталаза, регулирующий тканевое дыхание, тормозится антикаталазой. Возбуждение вызывает торможение, активность — покой и т. д.
В своеобразных взаимоотношениях находятся окончания тройничного и обонятельного нервов в слизистой оболочке носа. Слезотечение, кашель, чихание, вызванные химическим раздражением тройничного нерва, почти мгновенно прекращаются, если понюхать корочку хлеба, т.е. вызвать возбуждение обонятельных рецепторов.
Вся жизнь — в этом единстве противоположностей!
И ничего нет удивительного в том, что наряду с грубой, примитивной протопатической чувствительностью, возникшей много тысяч лет тому назад, на первых ступеням существования живых организмов, развилась в процессе эволюции вторичная, более тонкая, регулирующая и смягчающая система эпикритической чувствительности.
Как бы ни было едино и целостно болевое ощущение, все же оно складывается из отдельных, связанных между собой компонентов. Не исключено, что эпикритический и протопатический виды чувствительности и представляют две грани единого болевого комплекса.
Ведь из различных, с далеко неодинаковой физиологической значимостью отделов состоит единый нервный аппарат, из разных органов формируются единые системы пищеварения и кровообращения. Все это говорит скорее в пользу теории Гэда, чем против нее. Но наука накопила много новых фактов, не укладывающихся в старые концепции. Возможно, что и теория Гэда в чем-то устарела, в чем-то требует пересмотра.
Такова судьба многих научных открытий. На одном этапе они кажутся революционными, точными и не вызывающими сомнений. Но приходят новые исследователи с более тонкими методами научного анализа, по-новому освещают нередко давно известные факты, и все, что казалось столь ясным, обоснованным и доказанным, отходит в историю науки, уступая место совершенно неожиданным откровениям, непредвиденным толкованиям и непредусмотренным выводам.
Не будем же преждевременно сдавать в архив теорию Гэда. Она имеет как своих сторонников, так и противников. Будущее покажет, сохранится ли здоровое ядро этой теории, господствовавшей много лет в наших представлениях о формировании боли, или на смену ей придут истины, более веские и обоснованные.
Уже давно отзвучали споры между представителями корковой и подкорковой теории боли. Огромный экспериментальный и теоретический материал, накопленный в лабораториях и клиниках, показал, что каждая теория содержит и правильные, и неправильные положения. Конечное болевое ощущение формируется как в коре, так и в подкорковых образованиях головного мозга. Но различные мозговые структуры вносят свой вклад, включая свои «тоны и обертоны» в ту сумму раздражений, ощущений, эмоций, физиологических, физико-химических и патологических процессов, из которых складывается комплексное чувство боли.
Исследователи шли разными путями к решению вопроса о формировании болевого ощущения в различных участках мозга. Одни раздражали электричеством отдельные ядра, ансамбли нервных клеток и изолированные нейроны; другие действовали на них химическими веществами; третьи разрушали нервные структуры; четвертые предпочитали электроэнцефалографические записи; пятые, наконец, вводили в организм определенные фармакологические препараты и на фоне их действия изучали болевое поведение. Проводились бесчисленные эксперименты на животных — крысах, кроликах, собаках, обезьянах, ставились исследования на добровольцах, изучались болевые синдромы в клиниках. Шагом вперед явилось применение метода изучения болевых реакций, разработанного на кафедре психофизиологии Парижского университета.
Наибольший интерес представляют опыты, в которых сочетались физиологические, электроэнцефалографические, биохимические, неврологические и гистологические исследования.
Читателю уже известно, что и в эксперименте, и в клинике широко применяется метод отведения электрических потенциалов от различных отделов головного мозга. При помощи специальной аппаратуры удается зарегистрировать на бумаге или фотопленке электрические токи, возникающие в мозгу. Запись этих токов — электроэнцефалограмма — представляет сложную кривую, отражающую электрическую активность огромного числа нервных клеток. На ней можно выделить волны различной величины, частоты, формы. Чаще всего это так называемый альфа-ритм (8—13 колебаний в 1 сек.), который можно обнаружить в коре и подкорковых образованиях головного мозга. При различных воздействиях на организм альфа-ритм ослабевает, и величина ритмичных колебаний уменьшается. Это явление называется реакцией активации пробуждения, десинхронизации. Как правило, оно наблюдается также и при болевых раздражениях и наиболее выражено (по нисходящему ряду) в теменных, затылочных, височных и лобных долях мозга. Однако реакция пробуждения не специфична для боли. И нельзя ее считать объективным проявлением чувства боли. Аналогичная картина возникает при зрительных, слуховых, температурных и даже тактильных раздражениях.
Развитие техники и электроники значительно расширило возможности электроэнцефалографического исследования деятельности головного и спинного мозга. Этому в немалой степени способствовало внедрение в практику физиологического и даже клинического эксперимента метода вживления электродов в различные отделы центральной нервной системы. Почти в любой физиологической лаборатории удается без особого труда записать электрическую активность зрительных бугров, подбугорья, ретикулярной формации, гиппокампа, миндалевидного ядра и т.д.
При незначительной боли, вызванной слабым током, когда животное настораживается, иногда делает прыжок и очень редко убегает, никаких особых изменений в электроэнцефалограмме отметить не удается. Но сильная боль, сопровождающаяся прыжком, бегством, криком и попыткой укусить или сорвать электроды, вызывает отчетливое изменение электрической активности в разных отделах мозга, особенно отчетливо выраженную в гиппокампе. В нем при боли регистрируются токи высокой амплитуды, ритмом 6—7 в 1 сек. Изменения электрической активности гиппокампа длятся обычно 8—14 сек. и постепенно затухают. Одновременно в коре головного мозга и ретикулярной формации развивается типичная реакция пробуждения. Однако ни в том, ни в другом отделе мозга не удается обнаружить какие-либо специфические для боли сдвиги.
Применение различных болеутоляющих веществ (морфина, петидина, декстроморамида, производных салициловой кислоты) в сочетании с болевым раздражением во многом изменяет течение физиологических реакций и характер электроэнцефалограммы. Под влиянием морфина исчезают два компонента болевой реакции — крик и попытка укусить электроды. При этом в гиппокампе отсутствуют характерные изменения электрической активности.
У крыс с разрушенной ретикулярной формацией исчезают другие компоненты болевого поведения — настораживание, прыжок, бегство. Разрушение миндалевидного ядра напоминает действие морфина. Разрушение передней части зрительных бугров и коры лобных долей мозга снимает конечную поведенческую реакцию животного — попытку укусить или сорвать электроды.
На Симпозиуме по проблеме боли в Париже весной 1967 г. была предпринята попытка подытожить наши представления о формировании болевого ощущения в головном мозгу. Было заслушано и обсуждено много докладов, высказано немало интересных мыслей, сделано не меньшее число различных предположений. Можно считать установленным, что ретикулярная формация регулирует и контролирует более примитивные, вызванные болевым раздражением реакции настораживания, прыжка и бегства. Возбуждение ретикулярной активирующей системы вовлекает в процесс другие граничащие с нею отделы мозга. Зрительные бугры, в частности их медиальные (внутренние) ядра, являются центром более сложных эмоциональных, аффективных реакций. Переднее ядро зрительных бугров передает информацию, поступающую с периферии в кору головного мозга, где происходит осознание боли и вступают в действие сложные механизмы приспособительных функций. В коре происходит отбор и оценка поступающих импульсов, здесь формируется целенаправленное болевое поведение, цель которого перестроить функции организма в условиях неотвратимого болевого ощущения.
Разрушение некоторых отделов зрительных бугров резко усиливает реакцию на боль. Даже слабое болевое раздражение сопровождается криком и стремлением укусить или сорвать электроды. В некоторых случаях крыса приходит при этом в состояние настоящего бешенства. Это подтверждает уже неоднократно высказанное предположение, что зрительные бугры располагают тормозными системами, смягчающими болевое ощущение. Разрушение этих систем резко усиливает эмоциональные проявления боли.
В конце 70-х годов группа исследователей, среди которых следует назвать уже известного нам американского физиолога Лима и французских ученых Альб-Фессар, Кротамера и Делакура, широко разрабатывает вопрос о мозговых системах, смягчающих (демпфирующих) болевые ощущения. >>>На Парижском симпозиуме по боли о них говорил в своем докладе французский невропатолог Гарсен, а на симпозиуме по боли, который проходил в рамках XXIV Международного физиологического конгресса в Вашингтоне, выступили сами авторы этих интересных исследований.
В эволюционном развитии мозга от низших форм живых существ к высшим возникла необходимость как-то заглушать или ослаблять сигналы о сверхсильных импульсах, поступающих в центральную нервную систему. В некоторых случаях необходимо было затормозить поток сигналов, в некоторых — изменить их характер (модальность). Это привело к возникновению в центральной нервной системе нисходящей (афферентной — от центра к периферии) импульсации, оказывающей свое влияние на глубоколежащие мозговые образования или на периферические нервные пути. В своих статьях и докладах Альб-Фессар рисует сложные пути нисходящих или, как она их называет, тормозных болевых систем. Они состоят из определенных участков коры головного мозга (чувствительных, двигательных, теменных, отчасти лобных) и некоторых подкорковых образований, в первую очередь так называемого хвостатого ядра. Раздражение определенных участков хвостатого ядра электрическим током подавляет неприятный, тягостный характер импульсов, поступающих в мозг. Американские хирурги Эрвин, Браун и Марк использовали это наблюдение в клинической практике. Им удалось облегчить тяжелые боли, раздражая хвостатое ядро через вживленные электроды. В последние годы (1970—1972) составлена карта распределения в мозгу точек, раздражение которых вызывает полнейшее обезболивание. Некоторые исследователи утверждают, что, стимулируя эти точки электрическим током, они могли на животных производить сложнейшие операции без всякого наркоза.
Существование смягчающих боль систем в головном мозгу во многих отношениях соответствует современным представлениям о формировании болевого ощущения. Если вспомнить теорию Гэда о протопатической и эпикритической чувствительности, о способности коры головного мозга переводить болевые ощущения в «подболевые», то и представление о нисходящих «противоболевых» системах как бы воплотится в плоть и кровь. Мельзак утверждает, что существует специальный контролирующий механизм в ретикулярной формации мозгового ствола, оказывающий постоянное тормозящее влияние на всю систему синаптических передач — с импульсов от периферии до спинного и головного мозга. Альб-Фессар, а за ней и Гарсен высказывают мысль, что теоретически можно снимать боль, раздражая нисходящие системы мозга, но рассматривают эту возможность как «несбыточную мечту». Не будем такими пессимистами! Развитие современной нейрохирургии и хирургии боли не оставляет сомнении, что подобные операции найдут, если уже не нашли, свое место в клинической практике.
Кора лобных долей мозга принимает участие в организации поведения, наиболее выгодного для организма в условиях болевого раздражения. Именно в коре лобных долей происходит превращение боли в страдание. Как здесь не вспомнить парадоксальные результаты лоботомии, когда больные продолжали испытывать боль, но не страдали от нее. Однако в коре происходит не только формирование чувства боли и выработка наиболее выгодных при данной ситуации поведенческих реакций. В ней имеются также механизмы, облегчающие и подавляющие боль. Здесь расположены центры эпикритической чувствительности, отсюда осуществляется регулирующее влияние на ретикулярную формацию.
Важнейшую роль в формировании болевого ощущения играют процессы возбуждения и торможения, протекающие в различных структурах головного мозга. Особенное значение имеют они, как показали классические исследования школы И. П. Павлова, для деятельности коры головного мозга.
Сочетание и взаимодействие возбудительного и тормозного процесса позволяют животному ориентироваться в сложных положениях и разбираться в потоке поступающих из внешнего мира разнообразных раздражений.
В борьбе организма с болевым ощущением торможение играет чрезвычайно важную, если не решающую роль. «Клетки больших полушарий,— говорит И. П. Павлов [15],— в высшей степени чувствительны к малейшим колебаниям внешней среды и должны быть тщательно оберегаемы от перенапряжения, чтобы не дойти до органического разрушения. Таким ограничительным средством для клеток больших полушарий и является торможение».
Торможение дает клеткам мозга необходимый им отдых, способствует восстановлению их функций. Если раздражитель очень силен и превышает предел выносливости нервных клеток, он может привести последние к истощению и даже гибели. Эта угроза предотвращается своевременным развитием торможения, которое как бы ограждает нервные клетки от чересчур сильных воздействий, падающих на них из внешней или внутренней среды.
Несомненный интерес представляет в этом отношении так называемое запредельное, охранительное торможение, которое развивается при действии на организм чрезмерных раздражителей, даже условных.
Такие воздействия, как болезнь, перенапряжение, физическая боль, угрозы, психические потрясения и т.д., могут вызвать запредельное торможение (в особенности, если они действуют продолжительное время).
При запредельном торможении нарушается правило зависимости эффекта от величины и интенсивности раздражителя и сильные раздражители начинают действовать слабев умеренных. Это объясняется тем, что нервные клетки защищаются от истощения и разрушения при помощи широко распространяющегося процесса торможения.
Повседневная жизнь дает немало примеров стойкого запредельного торможения. Все мы из личного опыта знаем, какую острую, нестерпимую боль вызывают сравнительно небольшие нарушения целости тканей и как спокойно переносятся подчас чрезмерно сильные болевые раздражения. Торможение играет в этих случаях не только роль защитного фактора организма, но и своеобразного терапевтического средства.
Таковы отдельные этапы формирования единого, комплексного болевого ощущения, которое заставляет нас страдать, требовать помощи, стонать или кричать, иногда плакать. С большей или меньшей вероятностью мы подошли к пониманию его механизмов. Но анализ не будет полным, если мы пройдем мимо важнейшего — вегетативного отдела нервной системы, который не только выполняет приказы, поступающие из ее высших отделов, но и сам в значительной мере определяет состояние механизмов, регулирующих всю жизнедеятельность организма.
В специальной литературе это носит название «регуляция регуляторов». Вегетативная нервная система с ее центральными и периферическими образованиями, гуморальными и гормональными составными частями принимает самое энергичное участие во всех болевых процессах, организуя не только цепь болевых реакций, но и определяя характер самого болевого ощущения.
В мозгу, как мы уже знаем, существуют сложные вегетативные системы, которые приходят в деятельное состояние под влиянием медиаторов — ацетилхолина, адреналина или серотонина. Они и получили название холинергических, адренергических и серотонинергических структур. От их состояния в немалой степени зависит формирование болевого ощущения.
Введение в организм эзерина — вещества, подавляющего фермент холинэстеразу и тем самым усиливающего действие ацетилхолина,— изменяет в опытах на крысах соотношение компонентов болевого синдрома. Реакция бегства у крысы становится слабее, реакция крика и кусания электродов усиливается. Болевое возбуждение обостряется и удлиняется. Противоположное действие отмечается при введении холинолитического препарата — атропина. Стремление к бегству усилено, крик и кусание электродов ослаблены.
Однако немецкий ученый Герц, используя другие холинергические препараты (ареколин, треморин), пришел к выводу, что они ослабляют болевое ощущение и одновременно подавляют условно-рефлекторную деятельность крыс, т.е. действуют через высшие отделы головного мозга.
Шарпантье считает, что холинергические вещества осуществляют свое действие, возбуждая гиппокамп, а адренергические — ретикулярную формацию.
Советский фармаколог П. П. Денисенко также установил, что холин- и адренергические элементы лимбической системы, ретикулярной формации среднего мозга и подбугорья играют важную роль в формировании болевых реакций, причем, по его данным, ведущее значение имеют М-холинергические структуры. Ему удавалось во много раз усилить обезболивающее действие морфина, вводя его одновременно с препаратами, снижающими активность центральных М-холинергических образований. Однако следует признать, что вопрос о взаимоотношении холин- и адренергических систем в мозгу при формировании болевого ощущения далеко еще не ясен. Возможно, что у разных видов животных, а тем более у человека, роль их различна.
Еще менее ясен вопрос об участии серотонина в возникновении болевого ощущения. При полном освобождении головного мозга от серотонина или, напротив, при значительном увеличении его содержания в ткани мозга (то и другое легко осуществить с помощью определенных фармакологических препаратов) порог болевого ощущения резко изменяется, но подчас в одну и ту же сторону. По всей вероятности, серотонин контролирует в первую очередь эмоциональные реакции, обусловленные болью, и в гораздо меньшей степени затрагивает поведение животного, например реакцию кусания электродов.
Таким образом, можно предположить, что в центральной нервной системе существует два этажа (или, как говорят физиологи, два уровня), объединяющие болевые раздражения и превращающие их в чувство боли. На первом формируется состояние общей настороженности животного. Это происходит в ретикулярной формации и осуществляется ее адренергическими элементами. Здесь начало простых неспецифических ответов на боль, выражающихся в прыжке и бегстве. Возбуждение ретикулярной формации активирует кору головного мозга и вызывает в ней феномен пробуждения, т.е. подавление альфа-ритма.
На втором этапе, в лимбической системе (гиппокампе, миндалевидном ядре) и зрительных буграх развиваются специфические болевые реакции. Это ведет к возникновению эмоциональных, аффективных состояний. С этим уровнем у крысы связаны реакции крика и кусания электродов. Здесь действует холинергическая система. Центром ее является гиппокамп. В нее же входят некоторые участки зрительных бугров, но уже не возбуждающие, а тормозящие болевое ощущение.
Оба болевых уровня находятся под неослабным контролем коры головного мозга. Искусственное разрушение коры полностью снижает осмысленную реакцию, наблюдающуюся при болевом раздражении,— попытку укусить электроды, но не подавляет крика. Крик — прерогатива подкорки!
У человека кора превращает чувство боли в страдание, т.е. облекает болевой рефлекс в психическую оболочку. Переход боли в страдание необязателен, но, если он наступил, вся регуляция функций может оказаться под угрозой. Информация, поступающая в высшие отделы мозга, становится неточной в одних случаях, избыточной в других. Хаотическое пароксизмальное вмешательство высших нервных центров в физиологические процессы приводит к дезорганизации гомеостатических (приспособительных) механизмов, к возникновению невротических состояний. Цепь болевых реакций превращается в боль-болезнь.
Еще несколько лет тому назад на этом можно было бы поставить точку. Но за последние годы широкое звучание получила теория канадских ученых Мельзака и Уолла, известная в нашей стране под названием «теории входных ворот», или, точнее, «теории контроля афферентного входа». Мимо нее в настоящее время не проходит ни один исследователь, занимающийся проблемой боли. И в докладах, и в дискуссиях на симпозиумах 1973 г. в Ленинграде и Вашингтоне — многие неясные и нерешенные проблемы физиологии и, особенно, фармакологии боли рассматривались с точки зрения Мельзака.
По-видимому, теории интенсивности и специфичности не могут полностью расшифровать противоречивые аспекты болевого ощущения. Многие физиологи и фармакологи считают, что множество фактов, накопленных исследователями в эксперименте и клинике, не позволяют считать, что боль является специфической модальностью со своим исключительно обособленным рецепторным аппаратом, специальными путями проведения и центральными механизмами. В то же время и сторонники теории специфичности приводят множество неоспоримых фактов, подтверждающих существование анатомо-физиологической системы боли. Возможно, что правы и те и другие. Попыткой найти какую-то среднюю линию и является теория «входных ворот».
Мельзак и его сотрудники утверждают, что формирование болевого ощущения начинается в задних рогах спинного мозга. Здесь находятся нервные клетки, модулирующие импульсы, поступающие с периферии. Решающую роль в превращении или непревращении поступившего сигнала в болевой играет желатинозная субстанция. Она как бы «настраивает» клетки задних рогов, задает тон, включает определенные тоны и обертоны. Импульсы от рецепторов приходят в спинной мозг по толстым (А-бета) и тонким (А-дельта и С) волокнам, но проникают они в задние рога через «ворота» желатинозной субстанции. Одновременно нервные клетки задних рогов получают из вышележащих нервных центров нисходящие импульсы, аналогичные описанным выше «противоболевым», тормозным сигналам. На рис. 22 представлена схема Мельзака и Уолла, облегчающая понимание сложных процессов, разыгрывающихся у «ворот» центральной нервной системы.
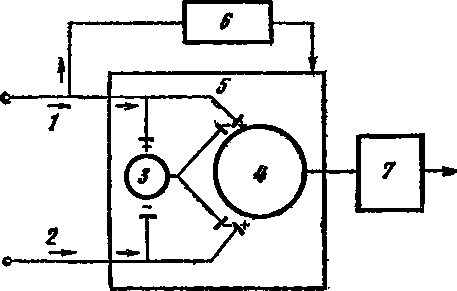
Рис. 22. Схематическая диаграмма теории «входных ворот» (по Мельзаку и Уоллу, 1965)
1 — толстое миелиновое волокно; 2 — тонкое безмиелиновое волокно; 3 — желатинозная субстанция; 4 — клетки центральной нервной системы, получающие первые афферентные сигналы; 5 — контроль, осуществляемый «входными воротами»; 6 — контроль, осуществляемый высшими отделами центральной нервной системы; 7 — система действия. Возбуждение +, торможение —. Торможение, которое оказывает желатинозная субстанция на клетки центральной нервной системы, усиливается импульсацией с толстых нервных волокон и ослабевает при импульсации с тонких нервных волокон. Центральные образования, контролирующие «входные ворота», возбуждаются под влиянием сигналов, поступающих по толстым нервным волокнам. Клетки центральной нервной системы стимулируют систему действия
Итак, клетки спинного мозга — так называемые передаточные клетки (ПК) — получают импульсы как по толстым, так и тонким нервным волокнам (1, 2). Импульсы модулируются желатинозной субстанцией (ЖС). Под ее влиянием они могут усиливаться (+) и ослабевать (—). Сигналы с толстых волокон подавляют передачу возбуждения (закрывают ворота), с тонких — активируют ее (открывают ворота). Импульс, поступивший по толстым волокнам («быстрая боль»), мгновенно оценивается высшими уровнями нервной системы. Эту оценку приводит специальная контролирующая система головного мозга. В тот момент, когда возбуждение в передаточных клетках спинного мозга достигло какого-то критического уровня, «входные ворота» открываются и происходит формирование болевого ощущения со всеми его болевыми и противоболевыми компонентами. При этом желатинозная субстанция действует в двух направлениях. Она способна блокировать импульсы, поступающие с периферии, и может способствовать образованию медиаторов в нервных клетках, тем самым усиливая или притормаживая проведение возбуждения в центральной нервной системе.
В дальнейшем Мельзак предпринял попытку расчленить единое болевое ощущение на три основных слагаемых. Физиологические особенности боли как одного из чувств (шестое чувство) регулируются спинно-бугровой системой, передающей импульсы с периферии в мозг. Мощная мотивационно-эмоциональная сфера боли связана с состоянием лимбико-ретикулярных структур мозга, которые побуждают живой организм совершать те или иные действия. И, наконец, познание, оценка боли и сопоставление ее с накопленным опытом совершается высшими отделами головного мозга, в первую очередь корой больших полушарий.
Таким образом, сигналы, поступающие от рецепторов, иногда достаточно сильные, чтобы вызвать боль, демпфируются и не доходят до сознания. В этом «повинна» желатинозная субстанция — либо вся, либо отдельные ее слои (пластины). Она придает им определенную модальность, которая может быть воспринята корой мозга и как ощущение прикосновения, и как чувство боли. В свою очередь сама центральная нервная система может затормозить превращение импульса в болевой, вводя в действие нисходящие противоболевые механизмы. Все это приводит к задержке иногда сильного, иногда даже сверхсильного импульса у «входных ворот» и к отсутствию болевого ощущения.
Теория Мельзака позволяет весьма убедительно объяснить действие некоторых противоболевых препаратов на организм. Быть может, поэтому она получила столь широкое распространение среди фармакологов, занимающихся проблемой обезболивания.
Теперь, как в любом математическом расчете, можно подвести некоторые итоги и подсчитать суммы прибылей и убытков. Формирование болевого ощущения — сложный, многозвеньевой процесс, охватывающий ряд анатомических и физиологических систем. Чувство боли возникает в результате системной деятельности нервной системы, т. е. вовлечения в действие самых различных ее формаций, ансамблей рецепторов, нейронов, секреторных клеток, периферических и центральных проводящих путей, различных как по строению, так и особенностями регулирования и химической передачи возбуждения. Функциональная система, реализующая болевое ощущение, включает и «болевые», и «противоболевые» механизмы, и смягчающие, и обостряющие боль настроечные компоненты, и пусковые, и выключающие элементы, Как и всякая функциональная система, болевая система «является конкретным физиологическим аппаратом, благодаря которому осуществляются саморегуляция и гомеостаз» [16].
Все эти факты и обобщения необходимо учитывать в борьбе с болью. Разумеется, не каждый лабораторный или клинический эксперимент может быть использован в медицинской практике. Но некоторые выводы из теоретических положений должны быть учтены и теоретиками, и врачами.
